近日,武汉纺织大学化学与化工学院朱君江教授团队,联合瑞士保罗谢勒研究所(PSI)等单位,在NH3选择性催化还原NO(NH3-SCR NO)反应机理研究方面取得新进展,揭示了Ce基催化剂上NH3-SCR NO 反应的关键决速步骤。相关成果以“The Role of Ce3+/Ce4+ Redox over Ce/TiO2 for the Selective Catalytic Reduction of NO with NH3”为题发表于ACS Catalysis。武汉纺织大学为第一署名单位,团队青年教师阳杰博士为论文第一作者,朱君江教授和Davide Ferri博士为论文通讯作者。

在NH3–SCR NO反应中,关于“催化反应的决速步骤”长期存在争议。围绕这一关键科学问题,研究团队构建了高度分散的Ce/TiO2催化剂体系,并结合瞬态反应、在线质谱及operando DR-vis光谱等手段,从动态角度解析了反应过程中Ce价态与反应速率之间的内在关联。
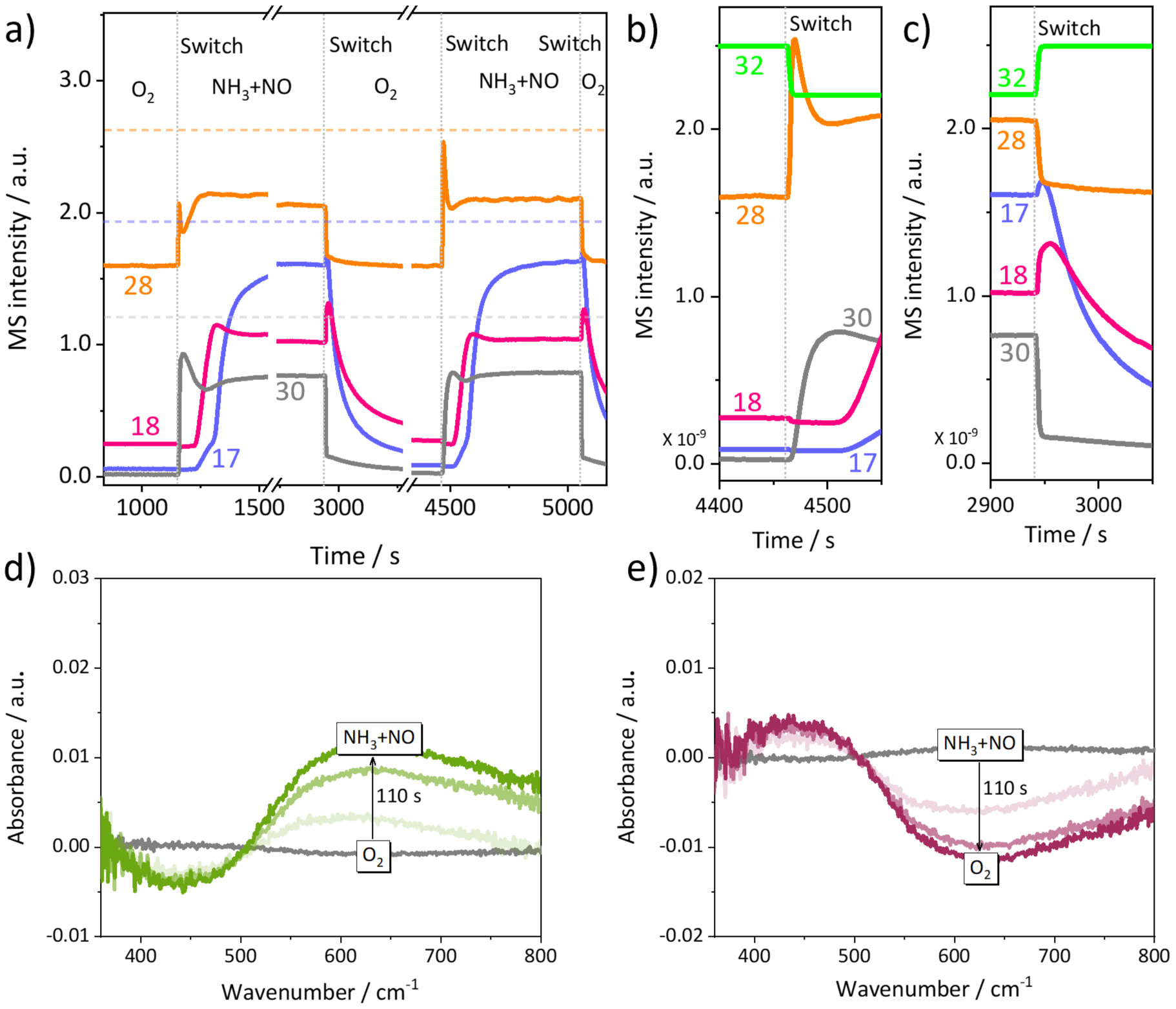
图1 operando DR-vis 揭示Ce3+/Ce4+在反应过程中的可逆动态转化
operando DR-vis结果显示(图1),NH3 + NO条件下,Ce4+被还原为Ce3+,引入O2后,Ce3+迅速被氧化为Ce4+,形成可逆的Ce3+/Ce4+循环。虽然在无O2条件下, NH3与NO仍可发生反应生成N2,但由于Ce3+无法被氧化,反应速率迅速衰减,说明催化循环受到限制。在O2与NH3 + NO交替切换过程中,观察到显著的N2“喷发”现象(N2 eruption)。该现象源于初始阶段表面Ce4+含量较高,反应短时间内不受Ce3+再氧化限制,因而表现出较高的反应速率。这一关键证据表明,限制反应持续进行的并非NO与NH3的反应步骤,而是Ce3+向Ce4+的再氧化过程。
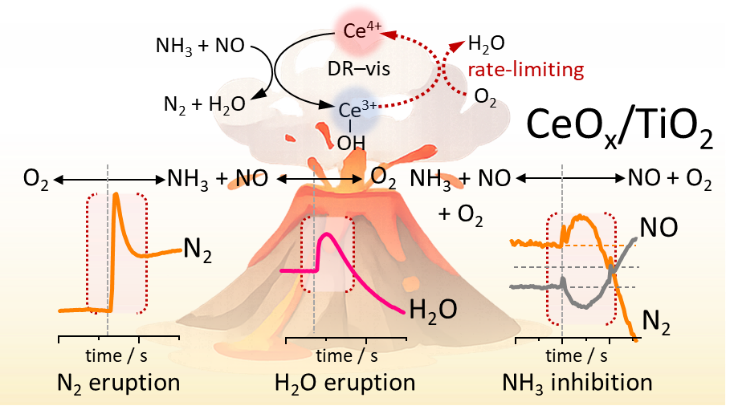
综合多种原位与瞬态实验结果,研究团队提出:在Ce/TiO2催化体系中,NH3–SCR NO反应遵循Eley–Rideal路径,而Ce3+向Ce4+的再氧化过程是控制反应速率的关键步骤。O2在反应中的核心作用并非直接参与反应,而是促进Ce3+再氧化,维持Ce3+/Ce4+氧化还原循环,从而保障催化反应的持续进行。该研究从动态与原位角度澄清了Ce基SCR催化剂中存在争议的决速步问题,为理解氧化还原循环在脱硝反应中的本质作用提供了直接证据,也为高效低温脱硝催化剂的设计提供了重要理论依据。
文章链接:https://doi.org/10.1021/acscatal.5c09137

